در این پست از سایت بنو قصد داریم کشف عوامل سرطان زا در نواحی بی فایده DNA را مورد بررسی قرار دهیم.
محققان موسسه گاروان از هوش مصنوعی برای شناسایی عناصر بالقوه سرطان زا در مناطق ” بیفایده ” DNA استفاده کرده اند و راه را برای روش های نوآورانه در تشخیص و درمان هموار کرده اند.
بر اساس یک مطالعه جدید از موسسه تحقیقات پزشکی گاروان، DNA غیر کد کننده – که 98 درصد از ژنوم ما را تشکیل می دهد و حاوی دستورالعمل هایی برای ساخت پروتئین نیست – ممکن است کلید تشخیص و درمان جدید سرطان باشد. این یافته ها که در مجله Nucleic Acids Research منتشر شده است، جهش هایی را در مناطقی از ژنوم که قبلا نادیده گرفته شده بودند نشان می دهد که ممکن است به شکل گیری و پیشرفت حداقل 12 سرطان مختلف از جمله سرطان پروستات، پستان و روده بزرگ کمک کند.
این کشف می تواند منجر به تشخیص زودهنگام و درمان های جدید موثر برای بسیاری از انواع سرطان شود.
دکتر آماندا خوری، افسر تحقیقات در Garvan و یکی از نویسندگان این مطالعه، می گوید: «DNA غیر کدکننده یک بار به دلیل عدم عملکرد آشکار آن به عنوان “DNA بیفایده ” رد شد. “تحقیقات ما جهش هایی را در این مناطق DNA پیدا کرده است که می تواند یک رویکرد کاملا جدید و جهانی برای درمان سرطان را باز کند.”
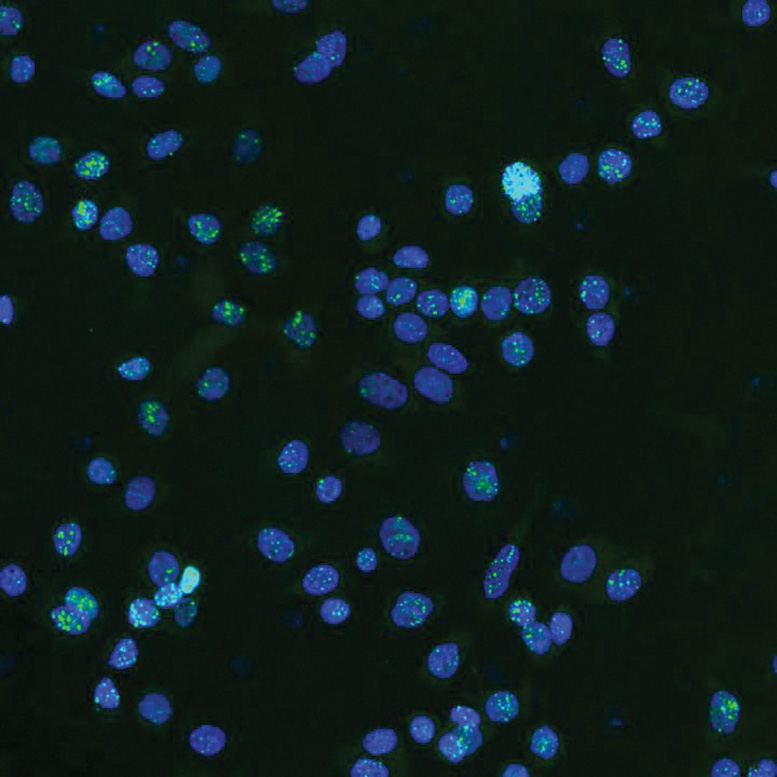
بررسی لنگرهای DNA مختل شده در سرطان
پژوهشگران بر روی جهشهایی که محلهای اتصال پروتئین CTCF را تحت تأثیر قرار میدهند تمرکز کردند. این پروتئین به تا کردن رشتههای بلند DNA به شکلهای خاص کمک میکند. در کار قبلی خود، آنها دریافتند که این مکان های اتصال بخش های دوردست DNA را به هم نزدیک می کنند و ساختارهای سه بعدی را تشکیل می دهند که کنترل می کنند کدام ژن ها روشن یا خاموش شوند.
دکتر خوری می گوید: “ما قبلا زیرمجموعه ای از مکان های اتصال CTCF را شناسایی کرده بودیم که “پایدار” هستند – یعنی آنها مانند لنگرهایی در ژنوم عمل می کنند که در انواع مختلف سلول وجود دارند. “ما این فرضیه را مطرح کردیم که اگر این لنگرها معیوب شوند، می تواند سازمان سه بعدی طبیعی ژنوم را مختل کند و به سرطان کمک کند.”
برای آزمایش این فرضیه، پژوهشگران یک ابزار جدید و پیچیده یادگیری ماشینی (AI) به نام CTCF-INSITE توسعه دادند که از ویژگیهای ژنومی و اپیژنومی برای پیشبینی محلهای اتصال CTCF که احتمالاً لنگرهای پایدار در مجموع ۱۲ نوع سرطان هستند،استفاده می کند. آنها سپس بیش از 3000 نمونه تومور از بیماران مبتلا به 12 نوع سرطان را که از پایگاه داده بین المللی کنسرسیوم ژنوم در دسترس است، ارزیابی کردند و دریافتند که لنگرهای پایدار سرشار از جهش هستند.
دکتر ونهان چن، نویسنده اول این مطالعه، می گوید: «با استفاده از ابزار یادگیری ماشینی خود، مکان های اتصال CTCF پایدار را در 12 نوع سرطان مختلف شناسایی کردیم. “به طور قابل توجهی، ما دریافتیم که هر نمونه سرطان حداقل یک جهش در یک محل اتصال CTCF پایدار دارد.”
“این تحقیق تأیید کرد که مکان های اتصال CTCF پایدار “نقاط داغ جهش” در سرطان ها هستند. ما فکر می کنیم این جهش ها به سلول های سرطانی مزیت بقا می دهند و به آنها اجازه می دهند تکثیر و گسترش یابند.
به سوی یک رویکرد جهانی درمان سرطان
این یافته ها می تواند پیامدهای گسترده ای برای درک و درمان بسیاری از انواع سرطان داشته باشد. پروفسور سوزان کلارک، رئیس آزمایشگاه اپی ژنتیک سرطان در گاروان و نویسنده اصلی این مطالعه، می گوید: «اکثر درمان های جدید سرطان باید به دقت جهش های خاصی را هدف قرار دهند که همیشه در میان انواع مختلف تومور رایج نیستند، اما از آنجایی که این لنگرهای CTCF در چندین نوع سرطان جهش یافته اند، ما امکان توسعه رویکردهایی را باز می کنیم که می تواند برای چندین سرطان موثر باشد.
محققان اکنون در حال برنامه ریزی آزمایش های بیشتر در مقیاس بزرگ با استفاده از ویرایش ژن CRISPR هستند تا بررسی کنند که چگونه این جهش های لنگر ژنوم سه بعدی را مختل می کنند و به طور بالقوه رشد سرطان را تقویت می کنند.
پروفسور کلارک می گوید: “اکنون که ما آنچه را که معتقدیم لنگرهای حیاتی ژنوم هستند کشف کرده ایم و نشان داده ایم که آنها برای حفظ هموستاز معماری ژنوم مهم هستند، منطقی است که این جهش های DNA غیر کد کننده این هموستاز را در سلول سرطانی مختل کنند – فرضیه ای که هنگام ویرایش آنها آزمایش خواهیم کرد.” “با مشاهده تأثیر پایین دست، ما امیدواریم که ژن های کلیدی یا مسیرهای ژنی را که تحت تأثیر جهش ها قرار می گیرند، شناسایی کنیم، که می تواند به عنوان نشانگر برای تشخیص زودهنگام سرطان یا اهدافی برای درمان های جدید عمل کند.”
او می گوید: «یافتن این سرنخ هایی که در حجم وسیعی از داده ها پنهان شده بودند، نمونه ای قدرتمند از چگونگی تقویت تحقیقات پزشکی هوش مصنوعی است. “این یک مرز کاملا جدید در مطالعه سرطان است و ما هیجان زده هستیم که آن را بیشتر بررسی کنیم.”
این تحقیق توسط کمک مالی شورای ملی بهداشت و تحقیقات پزشکی ایدهها و کمک مالی Investigator پشتیبانی شد.
برای اطلاعات بیشتر درباره این پروژه، میتوانید از مقاله منتشر شده آنها بازدید کنید.
اگه به مطالعه در مورد هوش مصنوعی و کاربرد های پزشکی آن علاقه مند هستید میتوانید پست قبلی سایت بنو ذر رابطه با ترکیب MEG و fMRI برای نقشهبرداری از دینامیکهای فضایی-زمانی مغز انسان در تشخیص یک تصویر بصری را مشاهده کنید:
نقشهبرداری از مسیرهای مغزی مربوط به بهیادآوری بصری
این پست برگرفته از جدیدترین اخبار SciTechDaily میباشد. منبع




بدون دیدگاه